Semana del 22 al 26 de Octubre
Semana del 16 al 19 de Octubre
Actividades de clase:
Desarrollo de actividades pendientes por resolver de la clase anterior.
Desarrollo del siguiente taller.
Una solución contiene 25 gr. de un compuesto
orgánico y 600 gr. de agua. Si el punto de ebullición de la solución
es 100,156°C, calcular el peso molecular del soluto.
Dato: Keb = 0,52 °C/m.
Dato: Keb = 0,52 °C/m.
Rsp: Masa Molar (soluto) =138,8 g/mol
Si se
disuelven 25 gr. de C6H10O5 en 250 gr. de
agua, calcular el punto de ebullición de la solución. Dato :PM del soluto
= 162 g/mol ;(Keb = 0,52 °C/m).
Rsp: Teb (solución) = 100,32°C
Una
solución acuosa de un soluto no volátil tiene un punto de ebullición igual a
100,204°C. Determinar la molalidad de la solución.
Rsp: m (solución) = 0,39
mol/Kg
Si se
prepara una solución de 9,99 gr. de CaCl2 (P.M. = 110 g/mol) en
162 gr. de agua, ¿cuál será el aumento en el punto de ebullición?
Dato: Keb = 0,52 °C/m
Rsp:
∆Teb (solución) = 0,29 °C
Si una
solución se prepara disolviendo 1,20 g de urea (Masa molar = 60 g/mol)
en 50 g de agua ¿ Cúal será el punto de ebullición y congelación de la solución resultante?
Para el agua Keb = 0,52 °C/m y Kc = 1,86 °C/m
Rsp: Teb (solución) = 100,208 °C y Tc (solución) = - 0,74°C
en 50 g de agua ¿ Cúal será el punto de ebullición y congelación de la solución resultante?
Para el agua Keb = 0,52 °C/m y Kc = 1,86 °C/m
Rsp: Teb (solución) = 100,208 °C y Tc (solución) = - 0,74°C
DISMINUCION DEL PUNTO DE
CONGELACION
Un cierto solvente congela a 76,3°C. Si se
disuelven 11 gr. de naftaleno (PM. = 128 g/mol) en 120 gr. de solvente, la
temperatura de congelación es 73,5°C.
Calcular la constante crioscópica del solvente.
Calcular la constante crioscópica del solvente.
Rsp: 3,90°C kg/mol
¿Cuántos gramos de etilenglicol ( CH2OHCH2OH
) se deben adicionar a 37,8 g de agua para dar un punto de congelación de
- 0.150° C ? Dato: Kc = 1,86 °C/molal
Rsp: 126.17 g
Se disuelve una tableta
de sacarina (C 7 H 4 SO 3 N
H) de 0,5 g en 250 mL de H2O. Calcular el pto.
de congelación y ebullición de esta disolución.
Rsp: Pto de congelación = - 0.02°C
Pto de ebullición = 100,006° C
Pto de ebullición = 100,006° C
Calcular el pto. de
congelación y ebullición de una disolución 0,30 molal de naftaleno
en benceno.
Datos: Kc benceno =5,12 º C/m ; Pto. de congelación del benceno = 5, 50º C , Keb = 2,53 ºC / m , Pto. de ebullición del benceno= 80,10 º C.
Datos: Kc benceno =5,12 º C/m ; Pto. de congelación del benceno = 5, 50º C , Keb = 2,53 ºC / m , Pto. de ebullición del benceno= 80,10 º C.
Rsp = 3,97º C y 80,86º C
Calcular
la Tº de congelación de una disolución anticongelante para automóviles.
El radiador de un automóvil contiene 7 Lt. de H2O ¿A qué Tº congelará el H2O si se le agregan 2.170 g de etilenglicol C2H 6O2 de masa molar = 62 g/mol, como anticongelante?
Dato: K c de H2O (constante crioscópica) es 1,86 ªC / mol .
Rsp: Pto. de congelación = - 9,3 ° C
DISMINUCION DE LA PRESION DE VAPOR
El radiador de un automóvil contiene 7 Lt. de H2O ¿A qué Tº congelará el H2O si se le agregan 2.170 g de etilenglicol C2H 6O2 de masa molar = 62 g/mol, como anticongelante?
Dato: K c de H2O (constante crioscópica) es 1,86 ªC / mol .
Rsp: Pto. de congelación = - 9,3 ° C
DISMINUCION DE LA PRESION DE VAPOR
Un mol de
glucosa se agrega a 10 moles de agua a 25°C. Si la presión de vapor del agua
pura a esta temperatura es de 23,8 mm Hg, ¿Cuál será la presión de la
mezcla?
Rsp: 21.66 mm Hg
El
naftaleno C10H8 , se utiliza para hacer bolas
para combatir las polillas. Suponga una solución que se hace disolviendo 0,515
g de naftaleno en 60,8 g de cloroformo CHCl3 , calcule el
descenso de la presión de vapor del cloroformo a 20° C en presencia de
naftaleno. La presión de vapor del cloroformo a 20° C es 156 mm
Hg. Se puede suponer que el naftaleno es no volátil comparado con el
cloroformo. ¿Cuál es la presión de vapor de la solución ?
Rsp: ∆P = 1,25 mm Hg; Pv (solución) = 154,75 mm Hg
Una solución líquida consiste en 0,35 fracciones
mol de dibromuro de etileno, C2H4Br2 y
0,65 fracciones mol de dibromuro de propileno, C3H6Br2 .
Ambos son líquidos volátiles ; sus presiones de vapor a 85° C son
173 mm Hg y 127 mm Hg, respectivamente. Calcule la presión de vapor
total de la solución.
Rsp: 143.1 mm Hg
PRESION OSMOTICA
Calcular la masa molar aproximada del pineno
sabiendo que al disolver 2,8 g en alcohol hasta un volumen de 500 mL se midió
una presión osmótica de 1,2 atm a 20 °C .
Rsp: 112 g/mol
Calcular la masa molar aproximada del tiofeno
sabiendo que una solución de 100 mL que contiene 0,32 g de ese compuesto en
alcohol dio una presión osmótica de 510 mm Hg a 20 °C
Rsp: 114,3
g/mol
¿Que presión osmótica en atm ejercerá cualquier
solución 0,1 M de una sustancia no ionizable a 20
°C?
Rsp: 2,40 atm
Actividades de clase:
Revisión y calificación del glosario.
Revisión y calificación de las actividades extraclase: Propiedades físicas, químicas y obtención de alcanos, alquenos y alquinos.
Revisión y calificación del glosario.
Revisión y calificación de las actividades extraclase: Propiedades físicas, químicas y obtención de alcanos, alquenos y alquinos.
Evaluación de cierre de competencia.
Inicio de competencia: Favor registrarla en el cuaderno.
Aplica los fundamentos de las reacciones orgánicas para
analizar la eficiencia de los diferentes métodos de obtención de los
compuestos orgánicos, basados en la estructura de sus grupos funcionales.
Contenido Temático:
PROPIEDADES Y OBTENCIÓN
DE ÁCIDOS CARBOXÍLICOS Y DERIVADOS: HALUROS DE ÁCIDO Y ESTERES
COMPUESTOS NITROGENADOS: AMIDAS Y AMINAS
Pregunta problematizadora:
¿Es posible utilizar algunas
sustancias químicas para evitar el desarrollo de hongos y bacterias en los
alimentos?
Explicación del tema
Desarrollo de ejercicios propuestos por la docente en clase.
1º Completar y nombrar, indicando el tipo de reacción y todos los posibles productos.
a.
b.
c.
d.
e.
f.
g.
p Benceno + Bromo gaseoso
q. Benceno + Acido Nítrico
t.
u. Benceno + Bromuro de isopropilo
a.
b.
c. Acido propanoico
d. Acido Etanoico
e. Cloruro de pentilo
f.
g.
h.
i.
j.
k.
l.
m.
n.
o.
p.
q.
r.
s.
t.
u.
v.
w.
x.
y.
z.
aa.
bb.
cc.
KMnO4
dd.
KMnO4
ee.
K2Cr2O7
ff.
K2Cr2O7
gg.
K2Cr2O7
hh.
K2Cr2O7
ii.
jj.
kk.
ll.
mm.
Semana del 8 al 12 de Octubre
Semana del 1 al 5 de Octubre
Las actividades extra clase se suspenden para dar prioridad a la semana de la cosecha. Espero mucho compromiso e interés en las actividades propuestas.
Actividades de clase:
11A:
No se programan actividades para ceder el espacio a las actividades de la semana de la cosecha.
11B:
La hora del viernes se cede para la ejecución de las actividades del día del estudiante.
En la clase del lunes se trabajará la química orgánica: Continuamos con las explicaciones y taller de propiedades físicas, químicas y obtención de alquinos. En clase se aplicará el quiz pendiente. Favor estudiar.
Semana del 24 al 28 de septiembre
Socialización de las pruebas RETOS del 3P.
Revisión y calificación de actividades extra clase.
Continuar con las explicaciones de:
Propiedades Colligativas
Propiedades y obtención de alquinos
Desarrollo de talleres y evaluación de los temas vistos. Favor estudiar.
Resolver los esjercicios propuestos en el siguiente link:
http://quimicadeliciosa.blogspot.com.co/2016/08/guia-de-ejercicios-propiedades.html
La presión de vapor del agua a 25°C es de 23,76 mmHg, calcular la disminución
de esta presión cuando a 24 moles de agua se le agregan 1 mol de glucosa. Cuál
es la presión de vapor de la solución?
Cual es la presión del agua a 23°C
cuando en 100 gr de ella se disuelven 5 gr de azúcar C12H22O11
Calcular el punto de ebullición de una
solución al 10% P/P de glucosa.
Si una solución acusa ebulle a 100.26°, su concentración molal, es?
Una solución que contiene 200 gr de H2O
y 9 gr de C6H12O6 congela a_______ °C y si se le agregan otros 9 gr de
soluto congela a _______ °C y ebulle a
_________ °C.
Una solución de NaCl cuya fracción molar es 0,4 tiene una presión de vapor de
________ Torr a 29°C (PH2O: 30 Torr)
La presión osmótica de una solución que contiene 18 gr de C6H12O6 en 100 ml de
solución a 27°C es __________ atm.
Actividades de clase:
Quiz de los temas vistos. Favor estudiar propiedades físicas y químicas de los alcanos.
Explicación y desarrollo de actividades respecto al tema de propiedades físicas y químicas de los alquenos y alquinos.
Socialización y compromisos de las actividades del día de la ciencia.
Semana del 10 al 14 de septiembre
Iniciamos................

Hola estudiantes:
Espero reflexionen sobre la necesidad de iniciar el cuarto período con todos los conceptos claros y las habilidades necesarias para comprender con facilidad los temas que cierran este año escolar.
Recuerden que un excelente desempeño no so logra el último día del período, éste es el resultado del esfuerzo y dedicación de 10 semanas (cerca de 50 días). Así que ánimo, ustedes pueden, cuentan con todo mi saber.
Espero reflexionen sobre la necesidad de iniciar el cuarto período con todos los conceptos claros y las habilidades necesarias para comprender con facilidad los temas que cierran este año escolar.
Recuerden que un excelente desempeño no so logra el último día del período, éste es el resultado del esfuerzo y dedicación de 10 semanas (cerca de 50 días). Así que ánimo, ustedes pueden, cuentan con todo mi saber.
Actividades de clase:
Iniciamos competencia: Favor registrarla en el cuaderno.
Comprende que los diferentes mecanismos de reacción
química (oxido-reducción, homólisis, heterólisis y pericíclicas) posibilitan la
formación de distintos tipos de compuestos orgánicos, para clasificar las reacciones orgánicas según el tipo de
ruptura, para predecir reactivos y/o productos teniendo en cuenta los mecanismos y agentes propios de cada ruptura,
resolviendo problemas y preguntas ICFES.
Contenido Temático:
REACCIONES ORGÁNICAS
Pregunta Problematizadora:
¿Cuáles son los tipos de
reacciones orgánicas que suceden en la naturaleza?
Explicación del tema:
Reacciones orgánicas.
Desarrollo del taller propuesto por la docente en clase.
Semana del 03 al 07 de septiembre de 2018
ACTIVIDADES DE CLASE:
Calificación de la dimensión Formativa: Favor traer organizado en el cuaderno la siguiente tabla:
VALORACIÓN DIMENSIÓN FORMATIVA
CRITERIO
|
AUTO
EVALUACION
|
COE
VALUACION
|
HETERO
EVALUACION
| |
1
|
Busco la excelencia en el desarrollo y presentación de tareas y trabajos.
| |||
2
|
Presento buena disposición en clase, soy atento y participativo.
| |||
3
|
Mantengo buena disciplina durante toda la clase.
| |||
4
|
Acato las normas de presentación personal establecidas por la Institución.
| |||
5
|
Cumplo oportunamente con las actividades extra clase.
| |||
TOTAL
|
Acciones de Mejora:
__________________________________________________________________________________________________________________________________________________
Acciones Correctivas:
__________________________________________________________________________________________________________________________________________________
__________________________________________________________________________________________________________________________________________________
Acciones Preventiva:
__________________________________________________________________________________________________________________________________________________
Aplicación de nivelaciones.
Socialización de desempeño final
Semana del 27 al 31 de agosto de 2018
ACTIVIDADES DE CLASE.
Evaluación de la dimensión formativa: Traer organizado el siguiente formato en el cuaderno:
VALORACION DIMENSION FORMATIVA
CRITERIO
|
AUTO
EVALUACION
|
COE
VALUACION
|
HETERO
EVALUACION
| |
1
|
Busco la excelencia en el desarrollo y presentación de tareas y trabajos.
| |||
2
|
Presento buena disposición en clase, soy atento y participativo.
| |||
3
|
Mantengo buena disciplina durante toda la clase.
| |||
4
|
Acato las normas de presentación personal establecidas por la Institución.
| |||
5
|
Cumplo oportunamente con las actividades extra clase.
| |||
TOTAL
|
Acciones de Mejora:
____________________________________________________________________________________________________________________________________
Acciones Correctivas:
____________________________________________________________________________________________________________________________________
____________________________________________________________________________________________________________________________________
Acciones Preventiva:
____________________________________________________________________________________________________________________________________
ACTIVIDADES DE CLASE.
Química Orgánica
Desarrollar en clase los siguientes ejercicios:
CETONAS:
ESTERES
Elabore las siguientes estructuras:
Escribe la fórmula estructural de los siguientes compuestos
a) 3-metil-2-butanol
b) 2-metil-1-propanol
c) 3,5-dimetil-4-heptanol
d) 5-etil-3-isopropil-2,2,5,6-tetrametil-3-heptanol
e) 4-ter-butil-6-etil-3,6,7-trimetil-4-octanol
f) 5-isopropil-7-metil-6-propil-3-nonanol
g) 2, 3,4-trimetil-3-hexanol
h) 3-etil-2,5-dietil-4-heptanol
i) 1,2-propanodiol
j) 5,7-dietil-2,2-dimetil-5-neopentil-4-nonanol
k) 1, 2,3-propanotriol
Escribe la fórmula estructural de cada unos de los siguientes éteres
:a) éter etil propílico
b) éter dimetílico
c) éter butil pentílico
d) éter isobutil metílico
e) éter etil isopropílico
f) 1-metoxipropano
g) 1-isopropoxi-2,2-dimetilbutano
Escribe las estructuras de los siguientes aldehídos y cetonas
a) etanal
b) pentanal
c) heptanal
d) 2-metilpropanal
e) 2,2-dimetilbutanal
f) 3-etil-2,3-dimetilhexanal
g) 2-pentanona
h) 4-nonanona
i) 3-hexanona
j) 3-metil-2-butanona
k) 3,3-dimetil-2-pentanona
l) 3-isopropil-4-metil-2-heptanona
m) 6-ter-butil-3-etil-7-metil-nonanona
Escribe las fórmulas estructurales de los siguientes ácidos carboxílicos.
a) ácido propanoico
b) ácido pentanoico
c) ácido metanoico
d) ácido octanoico
e) ácido 2,3-dimetilbutanoico
f) ácido 3,3-dimetilpentanoico
g) ácido 2,3,3-trimetilbutanoico
h) ácido 4-etil-3-isopropil-5-metiloctanoico
i) ácido 4,4-dietil-3-metilhexanoico
Escribe las fórmulas moleculares de los siguientes compuestos
a) 2-metilpropanamida
b) 3-etil-2,4-dimetilpentanamida
c) 2-etilbutanamida
d) etanamida
e) 3-isopropilhexanamida
f) 2,2-dimetilbutanamida
Escribe la fórmula estructural de las siguientes aminas.
a) 3-dimetilamino-4-etilhexano
b) 1-(etilamino)-3-metilpentano
c) 3-(etilmetilamino)pentano
d) 2-(dimetilamino)-4-metilpentano
e) 2-(etilpropilamino)-4-metilhexano
f) 2-(dietilamino)butano
g) 2-amino-3,4-dietil-5-metilhexano
h) 4-amino-3-etil-2-metilheptano
i) 2-(metilamino)-4-isopropil-2-metilheptano
Para resolver en clase:
QUÍMICA INORGÁNICA
1° Si 200 ml de una solución 0.5 M de KCl se diluyen en agua hasta un volumen de 1 L, la concentración final de la solución, es?
2° Cuantos ml de NaOH 1N neutralizaran 50 ml de H2SO4 1,3 N? Formula de Neutralización: VA.CA: VB. CB (VA: volumen del ácido, CA: Concentración del ácido, VB: Volumen de la Base, CB: Concentración de la base)
3°Para preparar 140 ml de H2SO4 0,75 N, el peso de ácido puro que se requiere, es?
4° 40 ml de HCl 0,15 N neutralizan justamente 29 ml de una solución de KOH. La concentración de esta solución, es?
5° Un estudiante desea preparar 100 ml de una solución de KI 0,5 M a partir de otra 2 M de la misma sal. Que volumen de esta última solución debe tomar?
6° Se desea evaporar cierta cantidad de solución de K2CO3 al 5% P/P con el fin de obtener 1 gr de la sal sólida. ¿Cuántos gramos de la solución se deben tomar para evaporar?
7° Al diluir 20 ml de HCl 0,12 M mediante la adición de 60 ml de agua, la concentración de la nueva solución, es?
8° Para cada uno de los siguientes casos determine el volumen de la solución concentrada que se debe tomar para preparar el volumen indicado de solución diluida:
Solución Concentrada Solución Diluida
a. NaCl 2M 200 ml de NaCl 0,4 M
b. Glucosa al 5% P/V 100 ml de glucosa al 2% P/V
c. HNO3 1,5 M 500 ml de HNO3 0,3 M
9° Se tiene 20 ml de solución 2 M de NaOH. Cuantos ml de agua se deben agregar para que la solución quede 0,5 M?
10° Dada la siguiente reacción:
a. Que volumen de HNO3 0,35 M reaccionara completamente con 275 ml de H2S 0,1 M?
b. Que peso de azufre se producirá a partir de 75 ml de HNO3 2,5 M
11° Cuantos ml de NaOH 0,5 M se requieren para reaccionar con 50 ml de ácido acético 0,1 M según la ecuación:
12° El cobre se disuelve en soluciones concentradas de acido nítrico en virtud de la reacción:
Cuantos gramos de cobre se disolverán en 20 ml de HNO3 6M?
13° Cual será la moralidad del NaOH en la solución que resulta al juntar 20 ml de NaOH 0,15 M con 80 ml de NaOH 0,05 M?
ACTIVIDADES DE CLASE.
QUÍMICA INORGÁNICA:
Retomamos las actividades normales de clase, como talleres, actividades para la casa y quices.
Terminar con el desarrollo de las evaluaciones iniciadas en la semana pasada.
Terminar con el desarrollo de las evaluaciones iniciadas en la semana pasada.
QUÍMICA ORGÁNICA:
Retomamos las actividades normales de clase, como talleres, actividades para la casa y quices.
Retomamos las actividades normales de clase, como talleres, actividades para la casa y quices.
Terminar con el desarrollo de las evaluaciones iniciadas en la semana pasada.
Terminar con el desarrollo de las evaluaciones iniciadas en la semana pasada.
Semana del 6 al 10 de agosto de 2018
ACTIVIDADES DE CLASE.
QUÍMICA INORGÁNICA:
Evaluación de competencia. Favor estudiar.
QUÍMICA ORGÁNICA:
Evaluación de competencia. Favor estudiar.Semana del 30 de julio al 3 de agosto de 2018
ACTIVIDADES DE CLASE.
QUÍMICA INORGÁNICA:
Continuar con las explicaciones de estequiometría aplicada a soluciones.
QUÍMICA ORGÁNICA:
Continuar con las explicaciones de Hidrocarburos aromáticos y Funciones de la química orgánica.
Semana del 23 al 27 de julio
ACTIVIDADES DE CLASE.
QUÍMICA INORGÁNICA:
Continuar con las explicaciones de dilución, estequiometría aplicada a soluciones y neutralización.
Continuar con las explicaciones de Hidrocarburos aromáticos y Funciones de la química orgánica.
Semana del 16 al 20 de julio
ACTIVIDADES DE CLASE.
socialización de los resultados de las pruebas aplicadas en el segundo período, acompañado de su respectivo análisis y proposición de acciones de mejora.
Continuar resolviendo la actividad propuesta la semana pasada respecto al tema de Soluciones y nomenclatura de Alquenos y alquinos. No olvides repasar desde casa, ya que semanalmente se aplicará un quiz de los temas vistos.
Semana del 9 al 13 de julio de 2018
QUE ALEGRÍA..........DE NUEVO A CLASES.............

Actividades de clase:
Encuadre pedagógico segundo semestre
Los talleres de clase, solo se califican en la respectiva clase. No después. Si el estudiante es ausente con excusa la nota del taller se le valora de otro taller en el que este presente.
Los talleres en lo posible se efectuarán de manera individual y se socializaran preguntado al estudiante de manera oral o escrita en el tablero.
Las actividades extra clase se califican en las fechas indicadas. No después. Para recibirla sustentada se hace necesario informar al padre de familia por medio de la agenda, indicando por escrito la fecha de la sustentación. Si reitera el incumplimiento con las actividades extra clase, entonces se citará al padre de familia para informarlo al respecto.
El cierre de la clase se hará por código de lista y su participación se registrará en la planilla de calificaciones.
Para estudiantes que reiteren más de un llamado de atención por pereza o distracción durante explicaciones o desarrollo de talleres, se les iniciará seguimiento con los respectivos compromisos y se les solicitará trabajar desde biblioteca el tema y actividades propuestas para la clase. Si esta situación es reiterada, se registrará en el observador con citación al padre de familia.
Cuando hayan desempeños bajos o básicos en pruebas escritas, se dará inicio a seguimiento académico, con el registro de los respectivos compromisos. Si es reiterado, se registrará en el observador con citación al padre de familia.
Estudiante que no cumpla con la presentación personal exigida por la institución, será reiterado del aula de clase para que resuelva dicha situación con el Coordinador de Convivencia.
Totalmente prohibido el uso del celular.
No se reciben por ningún motivo plantas para subir notas.
Las actividades de nivelación se harán en las fechas indicadas y en el aula de clase. No se repetirán en otros espacios. Excepto en el caso de estudiantes ausentes con excusa se les abrirá el posterior espacio.
El desempeño final del período se informará de manera definitiva en la fecha indicada luego de la realización de la actividad de nivelación y no tendrá modificaciones.
Las novedades de las clases se informarán por escrito al titular del curso.
RECUERDEN QUE USTEDES SON EXCELENTES ESTUDIANTES Y EN LA MEDIDA DE LA EXIGENCIA DEBEN RESPONDER A ESTAS ALTAS EXPECTATIVAS.
Actividades de clase:
Química Orgánica:
Competencia
Formula y nombra Hidrocarburos saturados, insaturados y
aromáticos, para comprender el lenguaje químico, aplicando las reglas de la
IUPAC.
Desarrollo de ejercicios:
Escriba las estructura de los siguientes alquenos
5-etil-2, 4,5-trimetil-3-hepteno
4-etil-3-isopropil-2-metil-3-hepteno
3-etil-4-isopropil-6,6-dimetil-3-hepteno
4-butil-5-isopropil-3,6-dimetil-3-octeno
7-terbutil-4-etil-9-isopropil-2, 4,10-trimetil-6-neopentil-5-propil-2-undeceno
Escriba la estructura de los siguientes alquinos
2-pentino
2, 2,5-trimetil-3-heptino
3-metil-1-butino
4,4-dimetil-2-hexino
2, 5,6-trimetil-3-octino
3-ter-butil-5-etil-1-heptino
Escribe las fórmulas estructuras de los siguientes derivados de alquilo
a) cloroetano
b) 2-cloropropano
c) 1,2-dibromoetano
d) 2-cloro-2-metilpropano
e) 2-cloro-3-etil-4-metilpentano
f) 1-cloro-2,2-dimetilpropano
g)1,3,5-triclorociclohexano
h) o-dibromobenceno
i) 4,4-difluoro-2-penteno
j) 1-cloro-3-metilciclobutano
QUÍMICA INORGÁNICA:
Semana del 28 de mayo al 1 de junio de 2018
Explicación de los temas:
Dilución
Neutralización
Estequiometría aplicada a soluciones
Desarrollo de ejercicios sobre los temas explicados propuestos por la docente en clase.
ACTIVIDADES DE CLASE:
Evaluación final de generalidades de la química orgánica.
Explicación de los temas:
Dilución
Neutralización
Estequiometría aplicada a soluciones
Nomenclatura de alcanos ramificados
Desarrollo de ejercicios sobre los temas explicados propuestos por la docente en clase.
Favor consignar en el cuaderno:
Pregunta Problematizadora:
¿Por qué el vinagre se le llama
también ácido etanoico?
Contenido Temático:
FUNCIONES QUÍMICAS Y GRUPOS FUNCIONALES DE LA QUÍMICA ORGÁNICA
Competencia:
Formula y nombra Hidrocarburos saturados, insaturados y
aromáticos, para comprender el lenguaje químico, aplicando las reglas de la
IUPAC.
Desarrollo del taller.
Escribe las estructuras de los siguientes alcanos ramificados
2-metilpropano
2, 2, 3-trimetilbutano
3-etil-2,3-dimetilhexano
5-ter-butil-5-etil-3-isopropil-2,6-dimetiloctano
4-sec-butil-2, 2, 4, 5,6-pentametilheptano
6-ter-butil-3, 5, 5-trietil-2,4-dimetilnonano
7-butil-6-isobutil-5-isopropil-3,8-dimetil-7-neopentil-6-propilundecano
Escriba las estructuras de los siguientes compuestos
3-ciclopentil-3-etilhexano
Isopropilciclohexano
Ciclohexilcilohexano
1, 1,3-trimetilciclobutano
1, 1, 2,2-tetrametilciclopropano
1,2-dimetilciclohexano
1-metil-2-propilciclooctano
Semana del 21 al 25 de mayo de 2018
ACTIVIDADES DE CLASE:
QUÍMICA ORGÁNICA
Desarrollo de actividades publicadas en la Semana del 30 de Abril al 4 de mayo de 2018.
Estudiar para quiz.
QUÍMICA INORGÁNICA
Evaluación de estequiometria aplicada a gases.
Taller de soluciones, publicado en el blog.
Quiz de los temas explicados
Semana del 14 al 18 de mayo de 2018
Revisión y calificación de la actividad extra clase. Favor resolverla sin falta, ya que se les han concedido tiempo de demás.
Estudiar los vídeos publicados de orgánica ya que se evaluarán en clase.
Evaluación de los temas explicados: Hibridación e hidrocarburos.
Evaluación de la estequiometría aplicada a gases. Estudiar sin falta.
Las exposiciones se suspenden, hasta estar al día con las demás actividades.
Favor tener el cuaderno al día, ya que se harán compromisos con los estudiantes, que presenten dos actividades en bajo en adelante.
Estudiar los vídeos publicados de orgánica ya que se evaluarán en clase.
Evaluación de los temas explicados: Hibridación e hidrocarburos.
Evaluación de la estequiometría aplicada a gases. Estudiar sin falta.
Las exposiciones se suspenden, hasta estar al día con las demás actividades.
Favor tener el cuaderno al día, ya que se harán compromisos con los estudiantes, que presenten dos actividades en bajo en adelante.
Semana del 7 al 11 de mayo de 2018
Revisión y calificación de la actividad extra clase solicitada desde la semana pasada, relacionada con una consulta sobre historia de la Química Orgánica.
Se continuará resolviendo las actividades pendientes publicadas la semana pasada sobre temas de orgánica.
Quiz de los temas vistos en clase sobre orgánica. Favor estudiar
QUÍMICA INORGÁNICA:
Se continuarán con las exposiciones, Favor tener en cuenta la exigencia y calidad esperada.
Se evaluará con un ejercicio el tema de estequiometría aplicada a gases.
Se continuará con la explicación del tema: Unidades físicas y químicas de concentración de las soluciones. Favor estudiar desde casa los ejercicios resueltos para quiz de ellos en clase.
Semana del 30 de Abril al 4 de mayo de 2018
QUÍMICA ORGÁNICA:
Competencia:
Clasifica los hidrocarburos según el tipo de enlace,
hibridación y tipo de cadena, para diferenciarlos de cada grupo de compuestos
según su estructura molecular, resolviendo preguntas ICFES.
ACTIVIDADES EXTRACLASE PARA LA SEMANA DEL 7 AL 11 DE MAYO
Haz una interesante lectura a las páginas 12 a la 14 del texto 11.1 Ed. Santillana (favor solicitarla a la docente) y resuelve en el cuaderno:
Científicos
|
Aporte
|
Importancia
|
Elementos que constituyen los compuestos orgánicos
| |||
Elemento
|
Abundancia
|
Compuestos
|
Importancia
|
Diferencias entre compuestos orgánicos e inorgánicos
| ||
Propiedad
|
Compuestos Orgánicos
|
Compuestos
Inorgánicos
|
Observa los siguientes vídeos:
Haz un breve resumen en el cuaderno, organizando las ideas en un mapa conceptual y estudia estos conceptos ya que serán evaluados en clase.
ACTIVIDADES DE CLASE:
Desarrollo de las siguientes actividades. Favor copiarlas al cuaderno. No se aceptan impresas.
1° Saturar las siguientes cadenas:
2° Completa la siguiente información:
Ejercicio
|
Fórmula Desarrollada condensada
|
Fórmula Molecular
|
Fórmula esquelética
|
a
| |||
b
| |||
c
| |||
d
| |||
e
| |||
f
|
3° Clasifica las siguientes cadenas en saturados o instaurados:
4° Clasifica las siguientes cadenas en: Aciclica (lineal o ramificada) Cíclica (homocíclica o heterocíclica)
5° Mediante el análisis de la formula molecular indique el tipo de hidrocarburo a los siguientes compuestos:
· C4H8
· C6H14
· C5H8
· C3H8
· C8H18
· C10H20
· C9H20
· C4H10
· C2H2
· CH4
6° Elabore la fórmula estructural, desarrollada, condensada, molecular y esquelética a los anteriores compuestos:
No.
|
f. estructural
|
F. desarrollada
|
F. condensada
|
F. molecular
|
a
| ||||
b
| ||||
c
| ||||
d
| ||||
e
| ||||
f
| ||||
g
| ||||
h
| ||||
I
| ||||
j
|
QUÍMICA INORGÁNICA:
Calificar y evaluar la actividad extra clase, relacionada con el tema de mezclas homogéneas o soluciones.
Resolver los ejercicios propuestos sobre: Unidades físicas y químicas de concentración de las soluciones.
Semana del 23 al 27 de Abril de 2018
ACTIVIDADES EXTRACLASE:
Resolver:
Con el ánimo de verificar tus saberes
alcanzados en la química estudiada durante la básica secundaria, lo invito
querido (a) estudiante a resolver el
siguiente interrogante. ¿Qué es una disolución?
Para facilitarte la respuesta, realiza esta
entretenida experiencia:
·
Mezcla en un recipiente un poco de agua y un poco de arena. Agita bien y
anota tus observaciones.
·
Mezcla en otro recipiente agua y un poco de azúcar, agita. Compara tus
observaciones con las del punto 1. ¿Hay diferencias? Enuméralas.
·
Analiza: ¿Qué método utilizaría para separar los componentes de las
mezclas 1 y 2?
·
Consulta en tu diccionario los términos homogéneo y heterogéneo. Cuál de
las dos mezclas es homogénea?, ¿Cuál aes heterogénea?
·
Las disoluciones son mezclas homogéneas de dos o más sustancias. Según
esto, ¿Cuál de las dos mezclas anteriores es una disolución?
·
El latón es una aleación de cobre y zinc; el bronce es una aleación de
cobre, zinc y estaño, de acuerdo con esto que entiendes por aleación? Es
correcto afirmar que las aleaciones son disoluciones? Por qué? Para qué sirven
las aleaciones?
·
El aire que respiras es una mezcla de nitrógeno, oxígeno y otros gases,
Se puede afirmar que el aire es una disolución? ¿Por qué?
·
Las disoluciones líquidas son las más conocidas. Escribe dos ejemplos de
ellas.
·
Observa a tu alrededor e identifica ejemplos de disoluciones sólidas y
gaseosas.
·
Las disoluciones son un estado intermedio entre mezclas y combinaciones.
Define con tus palabras mezcla, combinación y disolución. Escribe ejemplos de
cada una.
ACTIVIDADES DE CLASE:
Evaluación de la pregunta problematizadora del primer período. Favor reflexionar al respecto.
Explicación de los siguientes temas, con el desarrollo de ejercicios propuestos por la docente y quiz de los mismos:
Semana del 16 al 20 de Abril de 2018
ACTIVIDADES DE CLASE:
Socialización de las preguntas del simulacro aplicado el pasado 21 de marzo, con la finalidad de establecer acciones de mejora al respecto.
Exposición del proyecto investigativo del primer período.
Evaluación del tema: Estequiometría aplicada a gases. Favor reforzar el tema, ya que se observa poco interés por mejorar. Ya finalizado un período no se pueden hacer milagros para obtener un desempeño alto, este se logra día a día con trabajo y esfuerzo, no lo olviden.
Evaluación de la pregunta problematizadora del primer período. Favor reflexionar al respecto.
Explicación de los siguientes temas, con el desarrollo de ejercicios propuestos por la docente y quiz de los mismos:
Unidades físicas de concentración de las soluciones.
Semana del 9 al 13 de Abril de 2018
Socialización de las preguntas del simulacro aplicado el pasado 21 de marzo, con la finalidad de establecer acciones de mejora al respecto.
Tema: Estequiometría aplicada a gases.
Evaluar la pregunta problematizadora del primer período. Favor reflexionar al respecto.
Pregunta problematizadora:
¿De qué dependen las propiedades coligativas y qué importancia tienen en la cotidianidad y la industria?
Tema:
UNIDADES DE CONCENTRACIÓN DE LAS SOLUCIONES.
Competencia:
Establece
relaciones cuantitativas entre los componentes de una solución, para diferenciar las unidades químicas y
físicas de una concentración,
que le permitan resolver problemas de su cotidianidad, según operaciones
matemáticas.
Semana del 2 al 6 de abril de 2018
ACTIVIDADES DE CLASE.
Ev. ICFES DEL TEMA: LEYES DE LOS GASES
Revisión de actividades de nivelación a estudiantes con desempeño Bajo: Explicar los temas vistos de manera didáctica (estados de agregación y leyes de los gases) y grabarlo en un vídeo.
Para los desempeños Básico: Presentar sustentado las actividades pendientes y corrección sustentada de las evaluaciones con desempeño Bajo.
Evaluación de la dimensión formativa: Favor traer organizado en el cuaderno el siguiente formato.
VALORACION
DIMENSION FORMATIVA
CRITERIO
|
AUTO
EVALUACION
|
COE
VALUACION
|
HETERO
EVALUACION
|
|
1
|
Busco
la excelencia en el desarrollo y presentación de tareas y trabajos.
|
|||
2
|
Presento
buena disposición en clase, soy atento y participativo.
|
|||
3
|
Mantengo
buena disciplina durante toda la clase.
|
|||
4
|
Acato
las normas de presentación personal establecidas por la Institución.
|
|||
5
|
Cumplo
oportunamente con las actividades extra clase.
|
|||
TOTAL
|
Acciones de Mejora:
____________________________________________________________________________________________________________________________________
Acciones Correctivas:
____________________________________________________________________________________________________________________________________
____________________________________________________________________________________________________________________________________
Acciones Preventiva:
____________________________________________________________________________________________________________________________________
Semana del 19 al 23 de marzo de 2018
Felicitaciones a los estudiantes que cumplieron el compromiso de enviar el vídeo que explica el comportamiento de un gas:
María José Galeano. María José Soto, David Criales, María José Guzmán, Salomé Vasquez.
ACTIVIDADES DE CLASE:
Ev. ICFES DEL TEMA: LEYES DE LOS GASES
Explicación, taller y quiz del tema: Estequiometría aplicada a gases.
Semana del 12 al 16 de marzo de 2018
Jóvenes me tienen triste ya que no entiendo porque incumplen con las actividades extraclase. Ningún estudiante presentó el vídeo solicitado sobre una de las propiedades de los gases, por lo cual acumulan un desempeño bajo. Por favor mejorar ya que continúan con las mismas debilidades del año pasado. Reflexionar al respecto, ya que estos meses son decisivos para su futuro..........
Exposición de la noticia referente al problema de la contaminación atmosférica: Quema de basuras, entre otros. (Con evidencias y consulta de los efectos para el organismo de la emisión de estos gases).
Quiz de leyes de los gases. Favor estudiar y ver de nuevo el video, ya que será solo teoría.
Luego se evaluan ejercicios sobre las leyes de los gases, asi que es necesario repasar y prestar atención a las explicaciones.
Explicación del tema: Estequiometría aplicada a los gases. Favor reforzar el tema visto el año pasado, ya que ustedes presentaron bajo desempeño en el y espero que ya lo hayan superado.
Semana del 5 al 9 de marzo de 2018
ACTIVIDADES DE CLASE.
Exposición de la noticia referente al problema de la contaminación atmosférica: Quema de basuras, entre otros. (Con evidencias y consulta de los efectos para el organismo de la emisión de estos gases)
Explicación del tema: Leyes de los gases
Desarrollo del taller propuesto para la semana pasada.
Quiz de los temas.
ACTIVIDAD EXTRACLASE: Para ser resuelta en casa.
Experimentar las propiedades del estado gaseoso, con la realización de una sencilla experiencia: Grabar un vídeo con una duración de 2 minutos como máximo.
Masa
Volumen
Forma
Densidad
Movimiento
Estudiantes que se destacan durante la semana, felicitacionessssss
ACTIVIDADES DE CLASE:
Experimentar las propiedades del estado gaseoso, con la realización de sencillas experiencias:
Explicación del tema: Gases, propiedades y leyes, apoyados en el siguiente mapa conceptual y un vídeo:
Semana del 19 al 23 de febrero de 2018
ACTIVIDADES DE CLASE:
Masa
Volumen
Forma
Densidad
Movimiento
Presión
Organizados en grupos de tres estudiantes resolver los siguientes ejercicios:
1. En un recipiente de 1 L, a 2 atm de presión y 300 K de temperatura, hay 2,6 g de un gas. ¿Cuál es la masa molecular del gas?
2. La ley de Boyle establece que la presión y el volumen de un sistema gaseoso son inversamente proporcionales. Según esto, si aumentamos el volumen de un gas al doble, ¿qué le ocurre a la presión del mismo?
3. En el envase de cualquier aerosol podemos leer que no debemos arrojarlo al fuego ni aún vacío. ¿Por qué el fabricante está obligado a hacer esa advertencia? ¿En qué ley de los gases te basarías para explicar la advertencia?
4. Se introducen 3,5 g de nitrógeno, en un recipiente de 1,5 L. Si la temperatura del sistema es de 22 ºC, ¿cuál es la presión del recipiente? Si calentamos el gas hasta los 45 ºC, ¿cuál será la nueva presión si el volumen no varía?
5. Un gas ocupa un volumen de 250 mL a la temperatura de 293 K. ¿Cuál será el volumen que ocupe cuando su temperatura sea de 303 K? Enuncia la ley de los gases que usas para hacer el problema.
6. Qué volumen ocuparán 500 ml de un gas a 600 torr de presión si se aumenta la presión hasta 750 torr a temperatura constante?
7. ¿Qué presión hay que aplicar a 2,0 L de un gas que se encuentra a una presión de 1,0 atm para comprimirlo hasta que ocupe 0,80 L?
8. En un recipiente se tienen 16,4 litros de un gas ideal a 47ºC y una presión de una atmósfera. Si el gas se expande hasta ocupar un volumen de 22 litros y la presión se reduce a 0,8 atm, ¿cuál será la temperatura final del sistema?
9. Si cierta masa de gas contenido en un recipiente rígido a la temperatura de 100ºC posee una presión de 2 atm, ¿qué presión alcanzará la misma cantidad de gas si la temperatura aumenta a 473 K?
10.Si cierta masa de gas, a presión constante, llena un recipiente de 20 litros de capacidad a la temperatura de 124ºC, ¿qué temperatura alcanzará la misma cantidad de gas a presión constante, si el volumen aumenta a 30 litros
Quiz de leyes de los gases
Semana del 19 al 23 de febrero de 2018
ACTIVIDADES EXTRACLASE: Para la semana del 26 de febrero al 2 de marzo:
Experimentar las propiedades del estado gaseoso, con la realización de sencillas experiencias.
ACTIVIDADES DE CLASE
Revisión, socialización y calificación del proyecto de investigación.
Evaluación de competencia. Favor estudiar
Calificar las actividades extraclase asignadas la semana pasada.
Dramatizar el comportamiento de los sólidos, líquidos y gases, explicando con argumentos.
Explicación del tema: Gases, propiedades y leyes, apoyados en el siguiente mapa conceptual y un vídeo:
Explicación del tema: Gases, propiedades y leyes, apoyados en el siguiente mapa conceptual y un vídeo:
Organizados en grupos de tres estudiantes resolver los siguientes ejercicios:
1. En un recipiente de 1 L, a 2 atm de presión y 300 K de temperatura, hay 2,6 g de un gas. ¿Cuál es la masa molecular del gas?
2. La ley de Boyle establece que la presión y el volumen de un sistema gaseoso son inversamente proporcionales. Según esto, si aumentamos el volumen de un gas al doble, ¿qué le ocurre a la presión del mismo?
3. En el envase de cualquier aerosol podemos leer que no debemos arrojarlo al fuego ni aún vacío. ¿Por qué el fabricante está obligado a hacer esa advertencia? ¿En qué ley de los gases te basarías para explicar la advertencia?
4. Se introducen 3,5 g de nitrógeno, en un recipiente de 1,5 L. Si la temperatura del sistema es de 22 ºC, ¿cuál es la presión del recipiente? Si calentamos el gas hasta los 45 ºC, ¿cuál será la nueva presión si el volumen no varía?
5. Un gas ocupa un volumen de 250 mL a la temperatura de 293 K. ¿Cuál será el volumen que ocupe cuando su temperatura sea de 303 K? Enuncia la ley de los gases que usas para hacer el problema.
6. Qué volumen ocuparán 500 ml de un gas a 600 torr de presión si se aumenta la presión hasta 750 torr a temperatura constante?
7. ¿Qué presión hay que aplicar a 2,0 L de un gas que se encuentra a una presión de 1,0 atm para comprimirlo hasta que ocupe 0,80 L?
8. En un recipiente se tienen 16,4 litros de un gas ideal a 47ºC y una presión de una atmósfera. Si el gas se expande hasta ocupar un volumen de 22 litros y la presión se reduce a 0,8 atm, ¿cuál será la temperatura final del sistema?
9. Si cierta masa de gas contenido en un recipiente rígido a la temperatura de 100ºC posee una presión de 2 atm, ¿qué presión alcanzará la misma cantidad de gas si la temperatura aumenta a 473 K?
10.Si cierta masa de gas, a presión constante, llena un recipiente de 20 litros de capacidad a la temperatura de 124ºC, ¿qué temperatura alcanzará la misma cantidad de gas a presión constante, si el volumen aumenta a 30 litros
Quiz de leyes de los gases
Semana del 12 al 16 de febrero de 2018
ACTIVIDADES DE CLASE:
Revisión y calificación de la primera entrega del proyecto de investigación
Quiz de los temas vistos. Favor estudiar.
Explicar los estados de agregación.
Explicar las curvas de calentamiento y enfriamiento
Resolver las preguntas del siguiente link:
Socialización y calificación de las actividades extraclase.
ACTIVIDADES EXTRACLASE:
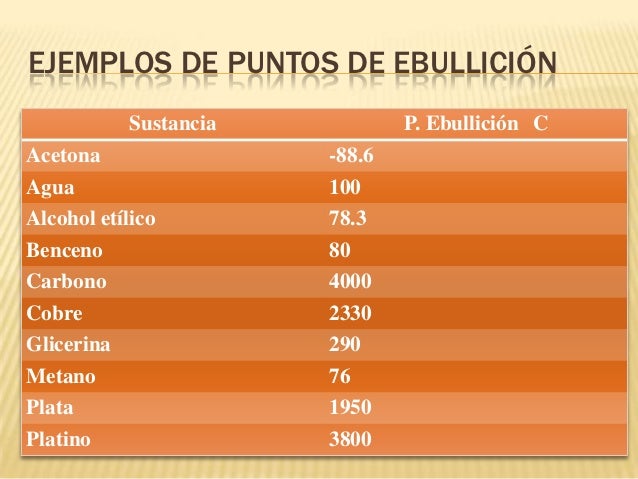
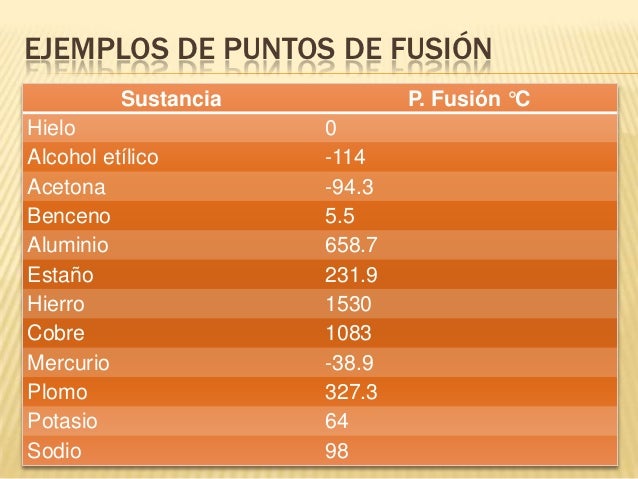
y observa las gráficas de los puntos de ebullición y fusión, luego completa la siguiente información. Por favor imprimir y pegar en el cuaderno dichas gráficas:
SUSTANCIA
|
PUNTO DE FUSIÓN
|
SUSTANCIA
|
PUNTO DE EBULLICIÓN
|
NAFTALENO
|
ETANOL
| ||
FRUCTOSA
|
CLOROX
| ||
PARAFINA
|
LECHE
| ||
AZÚCAR
|
VINAGRE
|
Observa la siguiente imagen y resuelve:
A qué temperatura ebulle el liquido? Señala también este punto de ebullición en la gráfica.
Resuelve:
Con base en la siguiente tabla, gráfica estos valores e indica a qué temperatura ebulle el líquido.
Observa la curva de calentamiento de agua y resuelve las siguientes preguntas:
Ingresa desde casa al siguiente link para tener un poco más claro lo que se realizará en clase.
Con los puntos de fusión y ebullición de las 5 sustancias consultadas y en compañía de tu docente, resuelve:
1. Realiza las gráficas de curvas de calentamiento de sustancias consultadas
2. Que es una curva de calentamiento
3. En que regiones aparecen los estados sólido, líquido y gaseoso de la
4. Que representan las líneas horizontales de la gráfica, que sucede en ellas
En la gráfica 1 y 2 Indique
1. la presencia de cada estado
2. Rangos de temperatura de cada estado
3. Puntos de fusión y ebullición
Gráfica 1 curva de calentamiento sustancia desconocida X
Gráfica 2 curva de enfriamiento sustancia desconocida Y
Queridos estudiantes, les deseo muchos éxitos en el presente año escolar 2018.
Recuerden y practiquen ....
Para tener en cuenta:
https://goo.gl/Fc3K2j
ACTIVIDADES DE CLASE
1°Presentación y explicación de pautas de la clase y criterios de evaluación del área.
Encuadre pedagógico:
Cada inicio o finalización de clase se aplicará un quiz, sea oral o escrito, individual o grupal.
Las actividades extraclase que no se entreguen en la fecha, se recibirán en la siguiente clase, sustentando una de las preguntas de la actividad asignada.
Los talleres de clase se califican en clase.
Actividades grupales para la casa no están autorizadas.
Para opinar o participar es necesario solicitar la palabra
Habrá acción reparadora para aquellos estudiantes que ingresen sin ninguna justificación luego de iniciada la clase.
Es necesario respetar a los compañeros y docente
Todos deben contribuir con la disciplina
Todos deben contribuir con el aseo del aula de clase
En las evaluaciones se sumará 0.5 a la calificación obtenida, si se evidencia buena ortografía y caligrafía.
El blog debe visitarse cada sábado para enterarse de las actividades de clase y extraclase.
Cualquier inquietud, favor comunicarla solo a través del blog.
2°Presentación y organización de la lista de clase.
3° Entrega de temas, competencias del período y pregunta problematizadora:
COMPETENCIA:
Experimenta las propiedades y leyes que rigen el comportamiento químico de los gases para realizar cálculos estequiométricos, según operaciones matemáticas
CONTENIDO TEMÁTICO:
GASES
PREGUNTA PROBLEMATIZADORA:
¿Qué importancia y utilidad tiene el estudio de los gases?
PROYECTO DE INVESTIGACIÓN:
¿Dibujar las capas atmosféricas y definir cada una.
Dibujar el mapa mundi localizando los países que mayor contaminación ejercen a la atmósfera.
Consultar los principales contaminantes químicos del aire y completar la información solicitada en la siguiente tabla:
Sustancia
contaminante
|
Composición/
Fórmula química
|
Fuente
natural
|
Efectos
|
Hacer lectura a una noticia de la actualidad en la que se informe problemas de contaminación del aire, para ser expuesta en clase.
Resolver las siguientes preguntas de inducción al tema:
a. Sustancias como el agua, la margarina de cocina, el chocolate, el hierro, entre otras se encuentran en fase sólida o estado sólido. De las anteriores sustancias, cuáles cambian de fase con un calentamiento leve?
b. Qué sustancias requieren altas temperaturas para lograr el cambio de fase?
c. Cuándo se dispone de una bebida a temperatura ambiente, por ejemplo a 20°C y si se desea fría, ¿qué se hace para enfriarla en pocos segundos? Por qué?
5° Interprete la siguiente información y resuelva:
Sustancia
|
Temperatura
|
Estado
|
5° Copie la imagen e Interprete la información suministrada y resuelva:
Elabore la gráfica que represente esta variación.
6° Explicación del tema, apoyado en la siguiente información:






































No hay comentarios:
Publicar un comentario